
目 次
雑科学ホーム
hr-inoueホーム
実 験
ドーピングをしていないアモルファスシリコン(i-a-Si)は、大阪大学基礎工学部の濱川研究室に於いて、シランのグロー放電分解によって作製した1),7),25),26)。a-Si作製装置の該略図を図1に示す。作製条件は表Iに示す通りである。
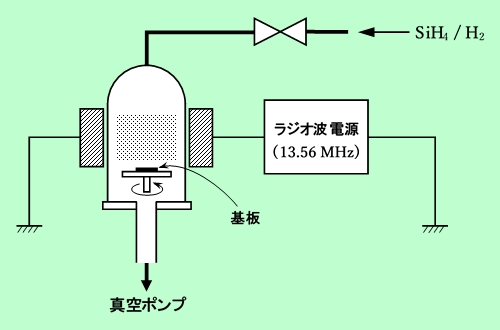
図1 アモルファスシリコン製造装置
表I a-Si薄膜作製条件
| 原料ガス |
SiH4(10%)/H2 |
| ガス流量 |
60 mL(STP)/min |
| 反応容器内圧力 |
0.9 Torr |
| 基板 |
ステンレス鋼
(表面粗さ10nm, 鏡面仕上げ) |
| 基板温度 |
225 ℃ |
| 電極-基板間距離 |
10 cm |
| ラジオ波周波数 |
13.56 MHz |
| ラジオ波出力 |
35 W |
| 膜生成速度 |
0.19 nm/sec |
a-Si膜の成長速度は、同じ条件下であらかじめガラス基板上にa-Si膜を作り、その膜の両面で反射される近赤外線(700〜2000nm)の干渉によって生じるパターンを解析することによって膜厚を求め、その値と放電時間とから算出する。それをもとにして放電時間を変化させると、任意の膜厚の試料が得られる。今回の実験では、膜厚はすべて500nmに統一した。このようにして作製したa-Si中には約20%の水素が含まれている。可視光の吸収スペクトルから、光学的バンドギャップは1.7eVであることがわかった。
反応容器から取り出した試料は暗所に保存する。これを電極として使用するには、次のようにする。裏側のステンレス鋼基板に銅線をウッド合金で接着し、この銅線を8mmφのガラス管に通す。表面のa-Si部分を残して裏側のステンレス鋼、銅線の部分をガラス管の先端と共にエポキシ樹脂で完全に覆う。エッチングを行なう場合には、この電極を5%フッ化水素酸に30秒間浸し、すぐにエタノールで洗浄、次いでヘキサンで洗浄した後に乾かして使用する。
電気化学的な測定を行なう装置の概略を図2に示す。白金対極は、1cm×1cm×0.5mmの板状のもので、飽和カロメル電極は自作である。電流は岩崎通信機製デジタルマルチメーターDM-3004を用いて測定した。また、電位の測定には、島津製作所製K-2型電位差計を用いた。電流-電位特性の測定は白金対極と飽和カロメル参照電極を用いた通常の三電極法で行なった。電流値はすべて定常状態になった後に読み取るようにする。また、光照射下の開放電圧の測定ではa-Siと白金対極との間の電圧を電位差計で直接読み取った。エッチング後の変化を追う場合以外は、これらの測定は、液中でa-Si電極と白金対極を短絡した状態で、暗状態で3時間放置した後に行なった。ただし、FeのEDTA錯体水溶液のみは電極の安定性が悪いので、短絡放置は30分間とした。
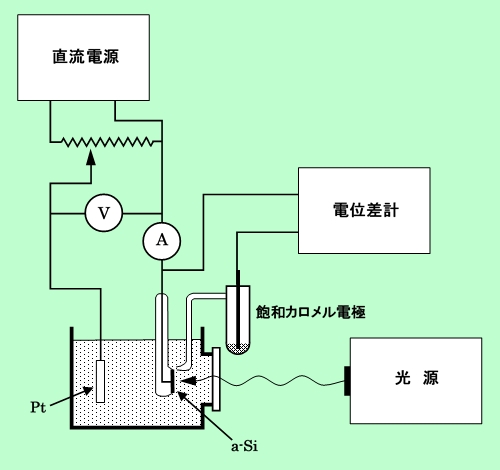
図2 測定装置
試薬は半井化学薬品製の特級のものを使用した。今回使用した水溶液の組成を表IIに示す。Fe(III/II)、ベンゾキノン(BQ)、及びヒドロキノン(HQ)の水溶液には、支持電解質として硫酸ナトリウムが加えてある。また、BQ、HQ水溶液は共に、調製後1日放置して電位の安定したものを使用する。これらの溶液では、調製直後は水や溶存酸素との反応で、それぞれ相手の化学種(BQではHQ、HQではBQ)が急速に生じて電位がかなり変化するが、1日放置するとその変化は非常に遅くなり、事実上問題なくなる。液の電位から判断して、約1%の相手の化学種が生成していると思われる。FeイオンのEDTA錯体の水溶液は、EDTAを溶解させるためにアンモニア水が加えてある。この溶液の場合はアンモニアが支持電解質としても働いている。各溶液のpH及び酸化還元電位、Eredoxの値も表IIに示してある。
表II 各水溶液の組成、pH、酸化還元電位
| |
組 成 |
pH |
酸化還元電位 |
| Fe(III/II) |
Fe2(SO4)3 |
0.05 M |
1.7 |
+0.35 V vs. SCE |
| FeSO4 |
0.1 M |
| Na2SO4 |
1 M |
| BQ |
C6H4O2 |
0.01 M |
5.5 |
+0.19 V vs. SCE |
| Na2SO4 |
1 M |
| HQ |
C6H4(OH)2 |
0.01 M |
5.5 |
+0.06 V vs. SCE |
| Na2SO4 |
1 M |
| Fe3+-EDTA/Fe2+-EDTA |
Fe2(SO4)3 |
0.025 M |
5.5 |
-0.13 V vs. SCE |
| FeSO4 |
0.05 M |
| Na2EDTA |
0.1 M |
| NH4OH |
|
目 次
雑科学ホーム
hr-inoueホーム


